Peptīdi ir savienojumu klase, kas veidojas, savienojot vairākas aminoskābes, izmantojot peptīdu saites.Tie ir visuresoši dzīvos organismos.Līdz šim dzīvos organismos ir atrasti desmitiem tūkstošu peptīdu.Peptīdiem ir svarīga loma dažādu sistēmu, orgānu, audu un šūnu funkcionālo aktivitāšu regulēšanā un dzīves aktivitātēs, un tos bieži izmanto funkcionālajā analīzē, antivielu pētījumos, zāļu izstrādē un citās jomās.Attīstoties biotehnoloģijai un peptīdu sintēzes tehnoloģijai, arvien vairāk peptīdu zāļu tiek izstrādātas un pielietotas klīnikā.
Ir daudz dažādu peptīdu modifikāciju, kuras var vienkārši iedalīt pēc modifikācijas un procesa modifikācijas (izmantojot atvasinātu aminoskābju modifikāciju) un N-termināla modifikāciju, C-termināla modifikāciju, sānu ķēdes modifikāciju, aminoskābju modifikāciju, skeleta modifikāciju, utt., atkarībā no modifikācijas vietas (1. attēls).Kā svarīgs līdzeklis, lai mainītu peptīdu ķēžu galvenās ķēdes struktūru vai sānu ķēdes grupas, peptīdu modifikācija var efektīvi mainīt peptīdu savienojumu fizikālās un ķīmiskās īpašības, palielināt šķīdību ūdenī, pagarināt darbības laiku in vivo, mainīt to bioloģisko sadalījumu, novērst imunogenitāti. , samazina toksiskās blakusparādības utt. Šajā rakstā ir aprakstītas vairākas galvenās peptīdu modifikācijas stratēģijas un to īpašības.
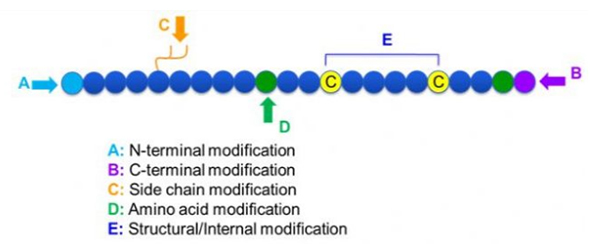
1. Riteņbraukšana
Cikliskiem peptīdiem ir daudz pielietojumu biomedicīnā, un daudzi dabiskie peptīdi ar bioloģisku aktivitāti ir cikliski peptīdi.Tā kā cikliskie peptīdi mēdz būt stingrāki nekā lineārie peptīdi, tie ir ārkārtīgi izturīgi pret gremošanas sistēmu, var izdzīvot gremošanas traktā un uzrāda spēcīgāku afinitāti pret mērķa receptoriem.Ciklizācija ir vistiešākais veids, kā sintezēt cikliskos peptīdus, īpaši peptīdiem ar lielu strukturālu skeletu.Atbilstoši ciklizācijas režīmam to var iedalīt sānu ķēdes sānu ķēdes tipā, terminālis - sānu ķēdes tips, termināls - termināla tips (tips no gala līdz galam).
(1) sānu ķēde uz sānu ķēdi
Visizplatītākais sānu ķēdes un sānu ķēdes ciklizācijas veids ir disulfīda tilts starp cisteīna atlikumiem.Šo ciklizāciju ievada cisteīna atlikumu pāris, kas tiek noņemti un pēc tam oksidēti, veidojot disulfīda saites.Policiklisko sintēzi var panākt, selektīvi atdalot sulfhidrila aizsarggrupas.Ciklizāciju var veikt vai nu pēcdisociācijas šķīdinātājā, vai uz pirmsdisociācijas sveķiem.Ciklizācija uz sveķiem var būt mazāk efektīva nekā ciklizācija ar šķīdinātāju, jo peptīdi uz sveķiem viegli neveido ciklizētas konformācijas.Cits sānu ķēdes - sānu ķēdes ciklizācijas veids ir amīda struktūras veidošanās starp asparagīnskābes vai glutamīnskābes atlikumu un bāzes aminoskābi, kas prasa, lai sānu ķēdes aizsarggrupa būtu iespēja selektīvi noņemt no polipeptīda. uz sveķiem vai pēc disociācijas.Trešais sānu ķēdes - sānu ķēdes ciklizācijas veids ir difenilēteru veidošanās ar tirozīnu vai p-hidroksifenilglicīnu.Šāda veida ciklizācija dabiskos produktos ir sastopama tikai mikrobu produktos, un ciklizācijas produktiem bieži ir potenciāla medicīniska vērtība.Šo savienojumu pagatavošanai nepieciešami unikāli reakcijas apstākļi, tāpēc tos bieži neizmanto parasto peptīdu sintēzē.
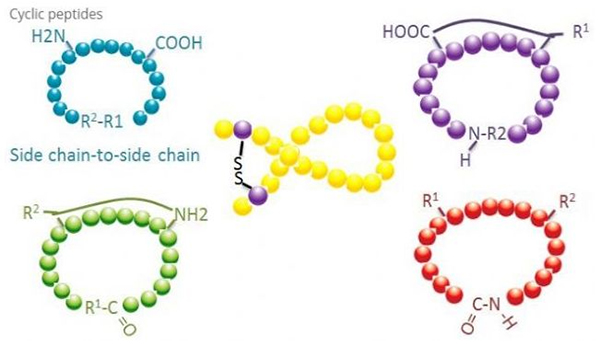
(2) no termināla uz sānu ķēdi
Termināla sānu ķēdes ciklizācija parasti ietver C-galu ar lizīna vai ornitīna sānu ķēdes aminogrupu vai N-galu ar asparagīnskābes vai glutamīnskābes sānu ķēdes ķēdi.Cita polipeptīdu ciklizācija tiek veikta, veidojot ētera saites starp C terminālu un serīna vai treonīna sānu ķēdēm.
(3) Termināls vai no galvas līdz astes tipam
Ķēdes polipeptīdus var vai nu ciklizēt šķīdinātājā, vai fiksēt uz sveķiem, izmantojot sānu ķēdes ciklu.Lai izvairītos no peptīdu oligomerizācijas, šķīdinātāju centralizācijā jāizmanto zemas peptīdu koncentrācijas.Sintētiskā gredzena polipeptīda iznākums no galvas līdz asti ir atkarīgs no ķēdes polipeptīda secības.Tāpēc pirms ciklisko peptīdu sagatavošanas lielā mērogā vispirms ir jāizveido iespējamo ķēdīto svina peptīdu bibliotēka, kam seko ciklizācija, lai atrastu secību ar vislabākajiem rezultātiem.
2. N-metilēšana
N-metilēšana sākotnēji notiek dabiskos peptīdos un tiek ievadīta peptīdu sintēzē, lai novērstu ūdeņraža saišu veidošanos, tādējādi padarot peptīdus izturīgākus pret bioloģisko noārdīšanos un klīrensu.Peptīdu sintēze, izmantojot N-metilētu aminoskābju atvasinājumus, ir vissvarīgākā metode.Turklāt var izmantot arī N-(2-nitrobenzolsulfonilhlorīda) polipeptīda-sveķu starpproduktu Mitsunobu reakciju ar metanolu.Šī metode ir izmantota, lai sagatavotu cikliskās peptīdu bibliotēkas, kas satur N-metilētas aminoskābes.
3. Fosforilēšana
Fosforilēšana ir viena no visizplatītākajām pēctranslācijas modifikācijām dabā.Cilvēka šūnās vairāk nekā 30% olbaltumvielu ir fosforilēti.Fosforilācijai, īpaši atgriezeniskajai fosforilēšanai, ir svarīga loma daudzu šūnu procesu kontrolēšanā, piemēram, signāla transdukcijā, gēnu ekspresijā, šūnu cikla un citoskeleta regulēšanā un apoptozē.
Fosforilāciju var novērot pie dažādiem aminoskābju atlikumiem, bet visizplatītākie fosforilēšanas mērķi ir serīna, treonīna un tirozīna atlikumi.Fosfotirozīnu, fosfotreonīnu un fosfoserīna atvasinājumus var ievadīt peptīdos sintēzes laikā vai veidot pēc peptīdu sintēzes.Selektīvu fosforilāciju var panākt, izmantojot serīna, treonīna un tirozīna atlikumus, kas selektīvi noņem aizsarggrupas.Daži fosforilēšanas reaģenti var arī ievadīt fosforskābes grupas polipeptīdā pēc modifikācijas.Pēdējos gados ir panākta vietai specifiska lizīna fosforilēšana, izmantojot ķīmiski selektīvu Staudingera-fosfīta reakciju (3. attēls).
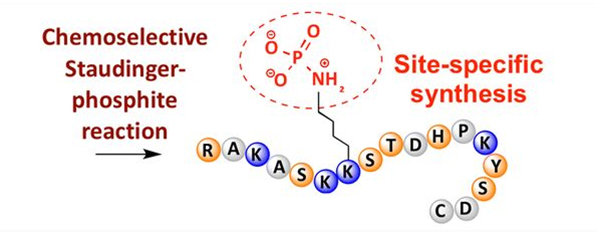
4. Miristoilēšana un palmitoilēšana
N-gala acilēšana ar taukskābēm ļauj peptīdiem vai proteīniem saistīties ar šūnu membrānām.Miridamoilētā secība N-galā ļauj Src ģimenes proteīnu kināzes un reversās transkriptāzes Gaq proteīnus mērķēt, lai tie saistīties ar šūnu membrānām.Miristīnskābe tika saistīta ar sveķu-polipeptīda N-galu, izmantojot standarta savienošanas reakcijas, un iegūto lipopeptīdu varēja atdalīt standarta apstākļos un attīrīt ar RP-HPLC.
5. Glikozilēšana
Glikopeptīdi, piemēram, vankomicīns un teikolanīns, ir svarīgas antibiotikas pret zālēm rezistentu bakteriālu infekciju ārstēšanai, un citus glikopeptīdus bieži izmanto, lai stimulētu imūnsistēmu.Turklāt, tā kā daudzi mikrobu antigēni ir glikozilēti, ir ļoti svarīgi pētīt glikopeptīdus, lai uzlabotu infekcijas terapeitisko efektu.No otras puses, ir konstatēts, ka proteīniem uz audzēja šūnu membrānas ir patoloģiska glikozilācija, kas liek glikopeptīdiem spēlēt nozīmīgu lomu vēža un audzēja imūnās aizsardzības pētījumos.Glikopeptīdus sagatavo ar Fmoc/t-Bu metodi.Glikozilētie atlikumi, piemēram, treonīns un serīns, bieži tiek ievadīti polipeptīdos ar pentafluorfenola estera aktivētu fMOC, lai aizsargātu glikozilētās aminoskābes.
6. Izoprēns
Izopentadienilēšana notiek uz cisteīna atlikumiem sānu ķēdē netālu no C-gala.Olbaltumvielu izoprēns var uzlabot šūnu membrānas afinitāti un veidot proteīna-olbaltumvielu mijiedarbību.Izopentadienētie proteīni ietver tirozīna fosfatāzi, mazo GTāzi, kočaperona molekulas, kodola slāni un centromērus saistošos proteīnus.Izoprēna polipeptīdus var pagatavot, izmantojot izoprēnu uz sveķiem vai ieviešot cisteīna atvasinājumus.
7. Polietilēnglikola (PEG) modifikācija
PEG modifikāciju var izmantot, lai uzlabotu olbaltumvielu hidrolītisko stabilitāti, bioloģisko sadalījumu un peptīdu šķīdību.PEG ķēžu ievadīšana peptīdos var uzlabot to farmakoloģiskās īpašības un arī kavēt peptīdu hidrolīzi ar proteolītisko enzīmu palīdzību.PEG peptīdi vieglāk nekā parastie peptīdi iziet cauri glomerulārā kapilāra šķērsgriezumam, ievērojami samazinot nieru klīrensu.Tā kā PEG peptīdu aktīvā pussabrukšanas periods in vivo ir pagarināts, normālu ārstēšanas līmeni var uzturēt ar mazākām devām un retāk lietojamām peptīdu zālēm.Tomēr PEG modifikācijām ir arī negatīvas sekas.Liels daudzums PEG neļauj fermentam noārdīt peptīdu, kā arī samazina peptīda saistīšanos ar mērķa receptoru.Taču PEG peptīdu zemo afinitāti parasti kompensē to garāks farmakokinētiskais pusperiods, un, ja PEG peptīdi atrodas organismā ilgāk, tiem ir lielāka iespēja uzsūkties mērķa audos.Tāpēc PEG polimēru specifikācijas ir jāoptimizē, lai iegūtu optimālus rezultātus.No otras puses, PEG peptīdi uzkrājas aknās samazināta nieru klīrensa dēļ, kā rezultātā rodas makromolekulārs sindroms.Tāpēc, ja peptīdus izmanto zāļu testēšanai, PEG modifikācijas ir jāizstrādā rūpīgāk.
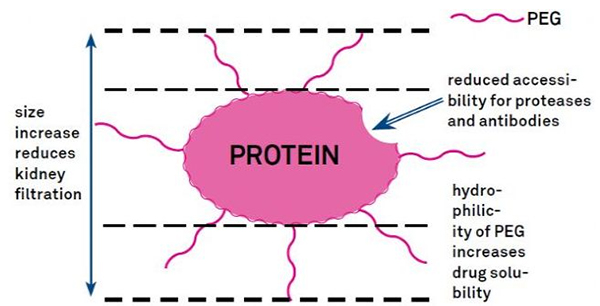
Kopējās PEG modifikatoru modifikāciju grupas var aptuveni apkopot šādi: amino (-amīns) -NH2, aminometil-Ch2-NH2, hidroksi-OH, karboksi-Cooh, sulfhidril (-tiols) -SH, maleimīds -MAL, sukcinimīda karbonāts - SC, sukcinimīda acetāts -SCM, sukcinimīda propionāts -SPA, n-hidroksisukcinimīds -NHS, akrilāts-ch2ch2cooh, aldehīds -CHO (piemēram, propionalds, butyrALD), akrila bāze (-akrilāts-acrl), biotiniloazīds, Biotīns, fluoresceīns, glutaril-GA, akrilāta hidrazīds, alkīnalkīns, p-toluolsulfonāts -OT, sukcinimīda sukcināts -SS utt. PEG atvasinājumus ar karbonskābēm var savienot ar n-gala amīniem vai lizīna sānu ķēdēm.Aminoaktivēto PEG var savienot ar asparagīnskābes vai glutamīnskābes sānu ķēdēm.Nepareizi aktivētu PEG var konjugēt ar pilnībā deaizsargātu cisteīna sānu ķēžu merkaptānu [11].PEG modifikatorus parasti klasificē šādi (piezīme: mPEG ir metoksi-PEG, CH3O-(CH2CH2O)n-CH2CH2-OH):
(1) taisnas ķēdes PEG modifikators
mPEG-SC, mPEG-SCM, mPEG-SPA, mPEG-OTs, mPEG-SH, mPEG-ALD, mPEG-butirALD, mPEG-SS
(2) bifunkcionāls PEG modifikators
HCOO-PEG-COOH, NH2-PEG-NH2, OH-PEG-COOH, OH-PEG-NH2, HCl·NH2-PEG-COOH, MAL-PEG-NHS
(3) sazarots PEG modifikators
(mPEG)2-NHS, (mPEG)2-ALD, (mPEG)2-NH2, (mPEG)2-MAL
8. Biotinizācija
Biotīns var būt stipri saistīts ar avidīnu vai streptavidīnu, un saistīšanās stiprums ir pat tuvu kovalentajai saitei.Ar biotīnu iezīmētos peptīdus parasti izmanto imūnanalīzē, histocitoķīmijā un plūsmas citometrijā, kuras pamatā ir fluorescence.Lai saistītu biotinilētus peptīdus, var izmantot arī marķētas antibiotīna antivielas.Biotīna etiķetes bieži tiek pievienotas lizīna sānu ķēdei vai N terminālam.6-aminokaproīnskābi bieži izmanto kā saiti starp peptīdiem un biotīnu.Saite ir elastīga, saistās ar substrātu un labāk saistās sterisku šķēršļu klātbūtnē.
9. Fluorescējoša marķēšana
Fluorescējošu marķējumu var izmantot, lai izsekotu polipeptīdus dzīvās šūnās un pētītu fermentus un darbības mehānismus.Triptofāns (Trp) ir fluorescējošs, tāpēc to var izmantot iekšējai marķēšanai.Triptofāna emisijas spektrs ir atkarīgs no perifērās vides un samazinās, samazinoties šķīdinātāja polaritātei, kas ir noderīga peptīdu struktūras un receptoru saistīšanās noteikšanai.Triptofāna fluorescenci var dzēst ar protonētu asparagīnskābi un glutamīnskābi, kas var ierobežot to izmantošanu.Dansilhlorīda grupa (Dansyl) ir ļoti fluorescējoša, ja tā ir saistīta ar aminogrupu, un to bieži izmanto kā aminoskābju vai olbaltumvielu fluorescējošu etiķeti.
Fluorescences rezonanse Enerģijas konversija (FRET) ir noderīga fermentu pētījumiem.Kad tiek izmantots FRET, substrāta polipeptīds parasti satur fluorescences marķēšanas grupu un fluorescences slāpēšanas grupu.Iezīmētās fluorescējošās grupas dzesē dzesētājs, izmantojot nefotonu enerģijas pārnesi.Kad peptīds tiek atdalīts no attiecīgā enzīma, marķēšanas grupa izstaro fluorescenci.
10. Būra polipeptīdi
Sprosta peptīdiem ir optiski noņemamas aizsarggrupas, kas pasargā peptīdu no saistīšanās ar receptoru.Pakļaujot UV starojumam, peptīds tiek aktivizēts, atjaunojot tā afinitāti pret receptoru.Tā kā šo optisko aktivāciju var kontrolēt atkarībā no laika, amplitūdas vai atrašanās vietas, būru peptīdus var izmantot, lai pētītu šūnās notiekošās reakcijas.Biežāk izmantotās aizsarggrupas būru polipeptīdiem ir 2-nitrobenzilgrupas un to atvasinājumi, kurus var ievadīt peptīdu sintēzē, izmantojot aizsargājošus aminoskābju atvasinājumus.Izstrādātie aminoskābju atvasinājumi ir lizīns, cisteīns, serīns un tirozīns.Tomēr aspartāta un glutamāta atvasinājumus parasti neizmanto, jo tie ir jutīgi pret ciklizāciju peptīdu sintēzes un disociācijas laikā.
11. Poliantigēnais peptīds (MAP)
Īsi peptīdi parasti nav imūni, un tie ir jāsavieno ar nesējproteīniem, lai ražotu antivielas.Poliantigēnais peptīds (MAP) sastāv no vairākiem identiskiem peptīdiem, kas savienoti ar lizīna kodoliem, kas var specifiski ekspresēt augstas iedarbības imunogēnus, un tos var izmantot, lai sagatavotu peptīdu nesēju proteīnu kuples.MAP polipeptīdus var sintezēt ar cietās fāzes sintēzi uz MAP sveķiem.Tomēr nepilnīga savienojuma rezultātā dažos zaros trūkst vai ir saīsinātas peptīdu ķēdes, un tādējādi tai nav sākotnējā MAP polipeptīda īpašību.Kā alternatīvu peptīdus var sagatavot un attīrīt atsevišķi un pēc tam savienot ar MAP.Peptīdu secība, kas pievienota peptīda kodolam, ir labi definēta un viegli raksturojama ar masas spektrometriju.
Secinājums
Peptīdu modifikācija ir svarīgs peptīdu izstrādes līdzeklis.Ķīmiski modificētie peptīdi var ne tikai uzturēt augstu bioloģisko aktivitāti, bet arī efektīvi izvairīties no imunogenitātes un toksicitātes trūkumiem.Tajā pašā laikā ķīmiskās modifikācijas var dot peptīdus ar dažām jaunām izcilām īpašībām.Pēdējos gados ir strauji attīstīta CH aktivācijas metode polipeptīdu pēcmodifikācijai, un ir sasniegti daudzi svarīgi rezultāti.
Izsūtīšanas laiks: 20.03.2023
